
|
|
HISTÓRIA DA TECNOLOGIA, TECNOLOGIA, OBJETOS AO REDOR DE NÓS
Dinamite. História da invenção e produção
Diretório / A história da tecnologia, tecnologia, objetos ao nosso redor A dinamite é uma mistura explosiva, um absorvente (por exemplo, kieselguhr) impregnado com nitroglicerina. Também pode conter outros componentes (salitre, etc.). A massa inteira geralmente é prensada em forma cilíndrica e colocada em embalagens de papel ou plástico. Minar a carga é realizada usando uma tampa de detonador. A dinamite foi patenteada por Alfred Nobel em 25 de novembro de 1867.
Por vários séculos, apenas um explosivo era conhecido pelas pessoas - pólvora negra, amplamente utilizada tanto na guerra quanto em explosões pacíficas. Mas a segunda metade do século XIX foi marcada pela invenção de toda uma família de novos explosivos, cujo poder destrutivo era centenas e milhares de vezes maior que o da pólvora. A sua criação foi precedida por várias descobertas. Já em 1838, Peluz realizou os primeiros experimentos sobre a nitração de substâncias orgânicas. A essência desta reação reside no fato de que muitas substâncias carbonáceas, quando tratadas com uma mistura de ácidos nítrico e sulfúrico concentrados, cedem seu hidrogênio, recebendo em troca o grupo nitro NO2 e se transformar em explosivos poderosos. Outros químicos investigaram esse fenômeno interessante. Em particular, Shenbein, algodão nitretado, recebeu piroxilina em 1846. Em 1847, agindo de forma semelhante sobre a glicerina, Sobrero descobriu a nitroglicerina, um explosivo com tremendo poder destrutivo. No início, a nitroglicerina não interessava a ninguém. O próprio Sobrero voltou aos seus experimentos apenas 13 anos depois e descreveu o método exato de nitração de glicerol. Depois disso, a nova substância encontrou algum uso na mineração. Inicialmente, ele era despejado no poço, tapado com argila e jateado por meio de um cartucho imerso nele. No entanto, o melhor efeito foi alcançado acendendo uma tampa de percussão com fulminato de mercúrio. O que explica o excepcional poder explosivo da nitroglicerina? Verificou-se que durante a explosão, ele se decompõe, como resultado do qual os gases CO são formados pela primeira vez2,CO,H2, CH4, N2 e NO, que novamente interagem entre si com a liberação de uma enorme quantidade de calor. A reação final pode ser expressa pela fórmula: 2C3H5(NÃO3)3 = 6CO2 + 5H2O+3N+0,5O2. Aquecidos a uma temperatura enorme, esses gases se expandem rapidamente, exercendo uma tremenda pressão sobre o meio ambiente. Os produtos finais da explosão são completamente inofensivos. Tudo isso parecia tornar a nitroglicerina indispensável para a detonação subterrânea, mas logo se descobriu que a fabricação, armazenamento e transporte desse explosivo líquido estava repleto de muitos perigos. Em geral, a nitroglicerina pura é bastante difícil de inflamar a partir de uma chama aberta. Um fósforo aceso apodreceu sem consequências. Mas, por outro lado, sua sensibilidade a choques e concussões (detonação) era muitas vezes maior que a do pólvora negra. Após o impacto, muitas vezes bastante insignificante, nas camadas submetidas à agitação, houve um rápido aumento da temperatura até que a reação explosiva começou. A mini-explosão das primeiras camadas produziu um novo impacto nas camadas mais profundas, e isso continuou até ocorrer a explosão de toda a massa de matéria. Às vezes, sem qualquer influência externa, a nitroglicerina de repente começou a se decompor em ácidos orgânicos, rapidamente escureceram, e então a agitação mais insignificante da garrafa foi suficiente para causar uma explosão terrível. Após vários acidentes, o uso de nitroglicerina foi quase universalmente proibido. Os industriais que lançaram a produção desse explosivo tinham duas opções: ou encontrar uma condição em que a nitroglicerina fosse menos sensível à detonação ou reduzir sua produção. Um dos primeiros que se interessou pela nitroglicerina foi o engenheiro sueco Alfred Nobel, que fundou uma fábrica para sua produção. Em 1864, sua fábrica decolou com os trabalhadores. Cinco pessoas morreram, incluindo o irmão de Alfred, Emil, que mal tinha 20 anos. Após esse desastre, a Nobel foi ameaçada com perdas significativas - não foi fácil convencer as pessoas a investir em um empreendimento tão perigoso. Por vários anos ele estudou as propriedades da nitroglicerina e finalmente conseguiu estabelecer uma produção completamente segura dela. Mas o problema do transporte permaneceu. Depois de muitos experimentos, Nobel descobriu que a nitroglicerina dissolvida em álcool é menos sensível à detonação. No entanto, este método não forneceu confiabilidade completa. A busca continuou e, em seguida, um incidente inesperado ajudou a resolver o problema de forma brilhante. Ao transportar garrafas de nitroglicerina, para suavizar o tremor, elas foram colocadas em terra de diatomáceas, uma terra de diatomáceas especial extraída em Hanover. Kieselguhr consistia em conchas de sílex de algas com muitas cavidades e túbulos. E uma vez, durante o transporte, uma garrafa de nitroglicerina quebrou e seu conteúdo caiu no chão. Nobel teve a ideia de fazer alguns experimentos com essa terra diatomácea impregnada de nitroglicerina. Descobriu-se que as propriedades explosivas da nitroglicerina não diminuíram pelo fato de ter sido absorvida pela terra porosa, mas sua sensibilidade à detonação diminuiu várias vezes. Nesse estado, não explodiu nem por atrito, nem por um golpe fraco, nem por queima. Mas, por outro lado, quando uma pequena quantidade de fulminato de mercúrio foi inflamada em uma cápsula de metal, ocorreu uma explosão da mesma força que deu nitroglicerina pura no mesmo volume. Em outras palavras, era exatamente o que era necessário, e até muito mais do que o Nobel esperava obter. Em 1867, ele tirou a patente de um composto que descobriu, que chamou de dinamite. O poder explosivo da dinamite é tão grande quanto o da nitroglicerina: 1 kg de dinamite em 1/50000 de segundo desenvolve uma força de 1000000 kgm, ou seja, suficiente para levantar 1000000 kg por 1 m. Além disso, se 1 kg de preto pó se transformou em gás por 0 segundos, depois 01 kg de dinamite em 1 segundos. Mas com tudo isso, a dinamite bem feita explodiu apenas com um golpe muito forte. Acendeu pelo toque do fogo, queimou gradualmente sem explosão, com uma chama azulada. A explosão ocorreu apenas quando uma grande massa de dinamite foi inflamada (mais de 0 kg). Minar dinamite, como a nitroglicerina, era melhor feito usando detonação. Para este propósito, Nobel no mesmo ano de 1867 inventou um detonador de primer chocalhante. A dinamite imediatamente encontrou a mais ampla aplicação na construção de rodovias, túneis, canais, ferrovias e outros objetos, o que predeterminou em grande parte o rápido crescimento da fortuna de seu inventor. Nobel fundou a primeira fábrica para a produção de dinamite na França, depois montou sua produção na Alemanha e na Inglaterra. Por trinta anos, o comércio de dinamite trouxe uma enorme riqueza ao Nobel - cerca de 35 milhões de coroas.
O processo de fabricação de dinamite foi reduzido a várias operações. Em primeiro lugar, era necessário obter nitroglicerina. Este foi o momento mais difícil e perigoso de toda a produção. A reação de nitração ocorreu quando 1 parte de glicerol foi tratada com 6 partes de ácido nítrico concentrado na presença de XNUMX partes de ácido sulfúrico concentrado. A equação ficou assim: C3H5(OH)3 +3HNO3 = C3H5(Eu não tenho3)3 + 3H2O. O ácido sulfúrico não participou do composto, mas sua presença foi necessária, em primeiro lugar, para absorver a água liberada como resultado da reação, que de outra forma, diluindo o ácido nítrico, impediria a completude da reação e, em segundo lugar, para isolar a nitroglicerina resultante de uma solução em ácido nítrico, pois, sendo altamente solúvel neste ácido, não se dissolveu em sua mistura com ácido sulfúrico. A nitração foi acompanhada por uma forte liberação de calor. Além disso, se, devido ao aquecimento, a temperatura da mistura subisse acima de 50 graus, o curso da reação seguiria na outra direção - a oxidação da nitroglicerina começaria, acompanhada de uma rápida liberação de óxidos de nitrogênio e aquecimento ainda maior , o que levaria a uma explosão. Portanto, a nitração teve que ser realizada com resfriamento constante da mistura de ácidos e glicerol, adicionando este último aos poucos e mexendo constantemente cada porção. A nitroglicerina formada diretamente em contato com ácidos, tendo uma densidade menor em comparação com a mistura ácida, flutuou para a superfície e pôde ser facilmente coletada após a conclusão da reação. A preparação da mistura ácida nas fábricas da Nobel acontecia em grandes vasos cilíndricos de ferro fundido, de onde a mistura entrava no chamado aparelho de nitração.
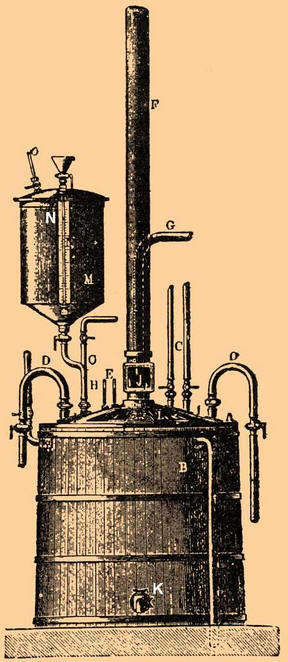
O aparato consistia em um recipiente de chumbo A, que foi colocado em uma cuba de madeira B e fechado com uma tampa de chumbo L, que foi untada com cimento durante a operação. As extremidades de duas bobinas de chumbo D, localizadas dentro do aparelho, passavam pela tampa (através delas era constantemente fornecida água fria). Ar frio também foi fornecido ao aparelho através do tubo C para agitar a mistura. O tubo F removeu os vapores de ácido nítrico do aparelho; o tubo G serviu para despejar uma quantidade medida da mistura ácida; glicerol foi derramado através do tubo H. No recipiente M foi medida a quantidade necessária dessa substância, que foi então injetada na mistura de nitrogênio por meio de ar comprimido admitido pelo tubo O. Nessa instalação, cerca de 150 kg de glicerol poderiam ser processados por vez. Depois de deixar entrar a quantidade necessária da mistura ácida e resfriá-la (passando ar comprimido frio e água fria pelas bobinas) a 15-20 graus, eles começaram a pulverizar a glicerina resfriada. Ao mesmo tempo, eles garantiram que a temperatura no aparelho não subisse acima de 30 graus. Se a temperatura da mistura começasse a subir rapidamente e se aproximasse do ponto crítico, o conteúdo da cuba poderia ser rapidamente liberado em um grande recipiente de água fria. A operação de formação de nitroglicerina durou cerca de uma hora e meia. Depois disso, a mistura entrou no separador - uma caixa retangular de chumbo com fundo cônico e duas torneiras, uma das quais localizada na parte inferior e a outra - na lateral. Uma vez que a mistura se assentou e se separou, a nitroglicerina foi liberada pela torneira superior e a mistura ácida pela parte inferior. A nitroglicerina resultante foi lavada várias vezes para remover o excesso de ácidos, pois o ácido poderia reagir com ela e causar sua decomposição, o que inevitavelmente levava a uma explosão. Para evitar isso, a água foi fornecida à cuba hermética com nitroglicerina e a mistura foi misturada com ar comprimido. O ácido se dissolvia em água e, como as densidades da água e da nitroglicerina eram muito diferentes, não era difícil separá-las. Para remover a água residual, a nitroglicerina foi passada através de várias camadas de feltro e sal de mesa. Como resultado de todas essas ações, obteve-se um líquido oleoso amarelado, inodoro e muito venenoso (a intoxicação pode ocorrer tanto pela inalação de vapores quanto pelo contato de gotas de nitroglicerina na pele). Quando aquecido acima de 180 graus, explodiu com uma força destrutiva terrível. A nitroglicerina preparada foi misturada com terra de diatomáceas. Antes disso, a terra de diatomáceas era lavada e completamente moída. A impregnação com nitroglicerina ocorreu em caixas de madeira forradas com chumbo no interior. Após mistura com nitroglicerina, a dinamite foi esfregada em uma peneira e colocada em cartuchos de pergaminho. Na dinamite kieselguhr, apenas a nitroglicerina estava envolvida na reação explosiva. Mais tarde, Nobel surgiu com a ideia de impregnar vários graus de pólvora com nitroglicerina. Nesse caso, a pólvora também participou da reação e aumentou significativamente a força da explosão. Autor: Ryzhov K.V.
▪ Fogo
Inaugurado o observatório astronômico mais alto do mundo
04.05.2024 Controlando objetos usando correntes de ar
04.05.2024 Cães de raça pura não ficam doentes com mais frequência do que cães de raça pura
03.05.2024
▪ Fontes de alimentação Cooler Master V Platinum 1300W ▪ O cérebro processa o que é aprendido no sono REM ▪ Notebook sem fonte de alimentação
▪ seção do site Audiotechnics. Seleção de artigos ▪ artigo de Lao Tzu. Aforismos famosos ▪ Como ocorreu a luta pelo renascimento da grandeza da França? Resposta detalhada ▪ artigo Proteção contra ruído ▪ Artigo Papel. Receitas e dicas simples
Página principal | Biblioteca | Artigos | Mapa do Site | Revisões do site www.diagrama.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese



 Veja outros artigos seção
Veja outros artigos seção 