
|
|
ENCICLOPÉDIA DE RÁDIO ELETRÔNICA E ENGENHARIA ELÉTRICA Características comparativas de elementos galvânicos de tamanho AA. Enciclopédia de rádio eletrônica e engenharia elétrica
Enciclopédia de eletrônica de rádio e engenharia elétrica / Carregadores, baterias, células galvânicas Hoje em lojas e mercados você pode encontrar muitas células galvânicas diferentes. Quais escolher? Este artigo irá ajudá-lo a tomar a decisão certa. Células galvânicas e baterias são amplamente utilizadas para alimentar vários equipamentos eletrônicos. Os elementos de tamanho AA são os mais amplamente utilizados. Nas prateleiras você encontra produtos similares de diferentes empresas, principalmente dois sistemas eletroquímicos: salino e alcalino. Mais recentemente, a Energizer lançou baterias de lítio AA de 1,5 V. A característica mais importante de uma célula galvânica - capacidade (a quantidade de eletricidade que ela é capaz de fornecer à carga) - quase nunca é indicada no rótulo. Resta ao comprador concentrar-se nos comerciais de televisão sobre as células que “funcionam até dez vezes mais que o sal convencional”, ou pegue a palavra da Energizer, que afirma que suas novas células AA de lítio e2 duram cinco vezes mais que as alcalinas convencionais [1 ]. Além disso, não está totalmente claro quais elementos são chamados de "comuns". Para comparar quantitativamente os parâmetros de elementos de diferentes sistemas eletroquímicos, é necessário testá-los nas mesmas condições. Tais testes foram realizados com três tipos de células: sal Philips Long Life (fem de uma célula "fresca" - 1,65 V), alcalina Duracell Ultra M1,62 (2 V) e lítio Energizer e1,8 (15 V). Cada um deles foi carregado com um resistor de 100 ohms, o que corresponde a uma corrente de descarga inicial de aproximadamente 1 mA. Para elementos de tamanho AA, essa corrente de carga é típica. A descarga foi realizada em ciclos de várias horas por dia, o que corresponde a condições reais de operação. Isso explica os picos de tensão nas curvas de descarga mostradas nas Figs. XNUMX. A curva azul corresponde ao elemento sal, vermelho - alcalino e verde - lítio. Durante o "repouso", a tensão no elemento de qualquer tipo aumentou ligeiramente, mas depois que a carga foi conectada, ela caiu rapidamente para o mínimo no ciclo anterior. Os pontos marcam os valores do EMF dos elementos - as tensões neles sem carga.
Se tomarmos como critério para a descarga completa da célula uma diminuição da tensão em sua carga para 0,9 V, a capacidade determinada experimentalmente da célula de sal foi de 1 Ah, a célula alcalina foi de 2,9 Ah e a célula de lítio foi de 3,5 Ah. Consequentemente, não há necessidade de falar sobre diferenças de cinco ou dez vezes na capacitância dos elementos de diferentes sistemas eletroquímicos. Na fig. 2 mostra outra série de curvas.
Eles mostram como a resistência interna dos elementos mudou durante o processo de descarga. A correspondência entre o tipo de elemento e a cor da curva é a mesma da Fig. 1. Os valores da resistência interna R, foram calculados pela fórmula
onde E é a EMF do elemento; U - tensão sob carga; RH é a resistência de carga. A resistência interna do sal e dos elementos alcalinos aumenta monotonicamente à medida que são descarregados. E a resistência do lítio, tendo diminuído drasticamente no início da descarga, permanece praticamente inalterada até o fim e depois aumenta com a mesma intensidade. Claro, os experimentos realizados não podem ser chamados de exaustivos. A capacidade de um elemento não é um valor estritamente fixo, depende de muitos fatores externos. Para diferentes elementos, seu máximo pode ser alcançado em condições de descarga significativamente diferentes. Para levar tudo isso em consideração, uma série muito grande de experimentos, irrealistas em condições amadoras, teria que ser realizada. No entanto, vamos tentar verificar os resultados obtidos por cálculo. Para estimar teoricamente a capacidade máxima possível de elementos de vários sistemas eletroquímicos, é necessário conhecer a composição química de seus eletrodos, eletrólito e a reação química que ocorre no elemento. Nas células salinas e alcalinas, o cátodo é o zinco e o ânodo é o dióxido de manganês. É por esta razão que tais elementos são chamados coletivamente de manganês-zinco. Mas o eletrólito neles é diferente: sal (geralmente cloreto de amônio) ou álcali (hidróxido de potássio). De acordo com [2], a reação ocorre em um elemento sal manganês-zinco
e em alcalino
Não há informações confiáveis sobre o material dos eletrodos e a reação química na célula de lítio. Podemos apenas supor que os eletrodos são lítio e dióxido de manganês, e o eletrólito é uma solução de perclorato de lítio em carbonato de propileno. Se esta conjectura estiver correta, conforme [2], a célula de lítio sofre a reação
Usando a lei de Faraday, obtemos uma expressão para determinar a capacitância de uma célula galvânica C, Ah:
onde m é a massa das substâncias reagentes F = 96,5-103 C/g-eq é o número de Faraday; n - valência (para sal e células galvânicas alcalinas - 2, para lítio - 1); M é o peso molecular total dos reagentes. Pesamos células galvânicas de tamanho AA: sal - 17 g, alcalino - 24 g, lítio - 15 g. ) é insignificante e pode ser desprezado. Calculamos o peso molecular total das substâncias reagentes a partir das equações de reações químicas acima: para sal - 346 g, para alcalino - 257 g, para lítio - 94 g. Substituindo valores numéricosna fórmula, obtemos o capacidade máxima possível do elemento sal - 2,6 Ah , alcalina - 5 Ah, lítio - 4,3 Ah. As diferenças entre os valores de capacitância calculados e os medidos podem ser explicadas por suposições bastante aproximadas feitas no cálculo. Portanto, diferenças de cinco e dez vezes não foram encontradas. A capacidade teórica de uma célula alcalina é cerca de duas vezes a de uma célula de sal, e o lítio não tem vantagem sobre a alcalina a esse respeito. Isto é consistente com os resultados experimentais. Com base nos resultados de todo o trabalho realizado, podemos concluir o seguinte: 1. As células galvânicas de lítio têm a tensão mais estável, a menor resistência interna, que praticamente não depende do grau de descarga, e a maior, embora não muito, capacidade. É preferível usá-los para alimentar equipamentos com grande consumo de corrente, bem como em dispositivos que desligam automaticamente quando a tensão de alimentação cai (por exemplo, câmeras digitais). 2. As células alcalinas têm uma capacidade comparável à do lítio e também são capazes de fornecer alta corrente à carga, mas a uma tensão mais baixa. Eles são mais usados em dispositivos com consumo médio de corrente sem controle automático de tensão. Em muitos casos, as pilhas alcalinas são preferidas ao lítio porque são três a quatro vezes mais baratas. 3. As células de sal têm a menor capacitância e a maior resistência interna. É aconselhável utilizá-los em equipamentos com baixo consumo de corrente. Literatura
Autor: I.Podushkin, Moscou
Couro artificial para emulação de toque
15.04.2024 Areia para gatos Petgugu Global
15.04.2024 A atratividade de homens atenciosos
14.04.2024
▪ Estrada de plástico feita de garrafas recicladas ▪ Drivers ISSATA LED para luminárias Armstrong ▪ Fontes de alimentação de segurança Mean Well PSC-160 ▪ Dispositivo a laser que produz partículas com massa negativa
▪ seção do site Materiais de referência. Seleção de artigos ▪ artigo E em todos os lugares paixões fatais, e não há proteção contra o destino. expressão popular ▪ artigo Por que os americanos são chamados de Pindos? Resposta detalhada ▪ artigo IrDA faça você mesmo. Enciclopédia de rádio eletrônica e engenharia elétrica ▪ artigo Modernização do transceptor RA3AAE. Enciclopédia de rádio eletrônica e engenharia elétrica
Comentários sobre o artigo: convidado Artigo explicativo, obrigado.
Página principal | Biblioteca | Artigos | Mapa do Site | Revisões do site www.diagrama.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese






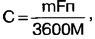
 Deixe seu comentário neste artigo:
Deixe seu comentário neste artigo: